
香港文匯報訊(記者 楊梓穎)香港科技大學(科大)生命科學部副教授郭玉松領導的研究團隊,在理解細胞如何管理蛋白質內部運輸的機制方面取得重大突破。研究指出,分泌運輸路徑如同細胞的「郵政服務」,確保蛋白質被準確送達目的地以維持細胞正常功能;一旦出錯,可能導致嚴重生理缺陷,並與多種遺傳性疾病密切相關。相關成果已於國際知名期刊《美國國家科學院院刊》(PNAS)發表。
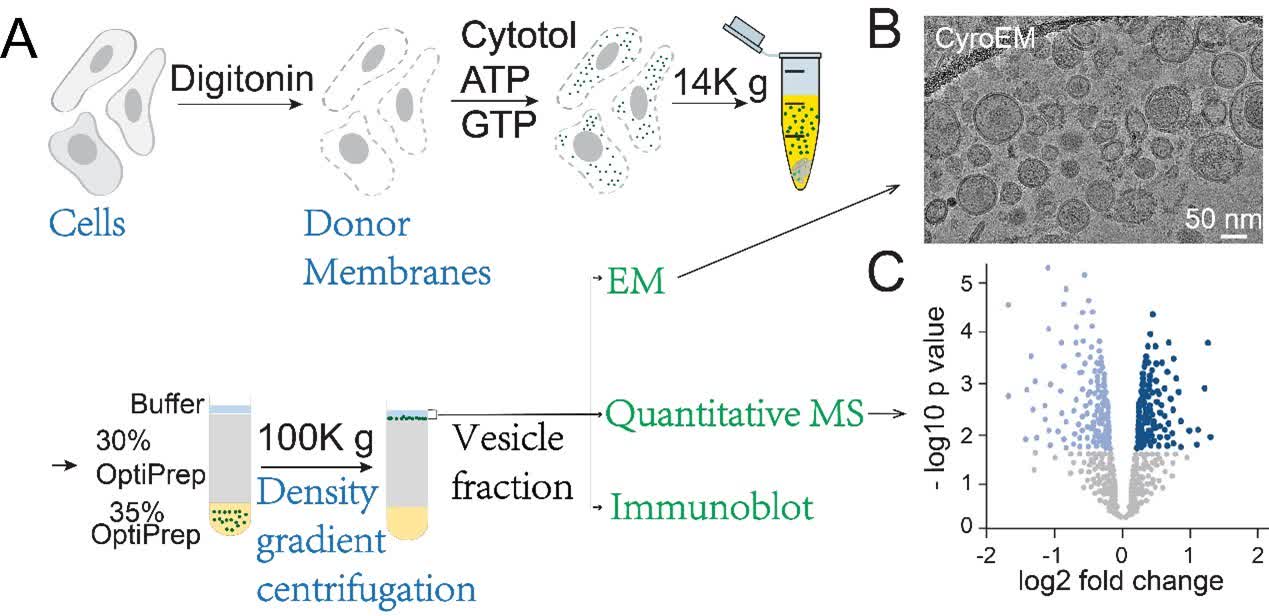
研究團隊透過創新的囊泡蛋白質組學平台進行系統性分析,成功識別與兩種關鍵細胞運輸複合體AP-1與AP-4相關的新型運送蛋白及其關鍵輔助因子並繪製出前所未見的運送蛋白與調控因子的完整圖譜。
郭玉松表示,科學界長期致力於全面繪製適配複合體如AP-1及AP-4的運送蛋白組,原因在於這些複合體的功能失常與多種嚴重遺傳疾病有直接關係,包括MEDNIK綜合症、X染色體相關智力障礙,以及AP-4缺陷綜合症等。
他進一步解釋,團隊透過在體外重構運輸過程並應用定量蛋白組學,讓研究能「直接識別」哪些蛋白質需要依賴AP-1或AP-4才能被包裝進囊泡,令研究視角由以往分散、零碎的認知,轉向對運輸全貌的整體掌握,並揭示新的客戶蛋白與AP-4所依賴的、意想不到的細胞機制。
該團隊的創新方法將體外囊泡重組與定量質譜分析技術相結合,讓研究人員能夠在受控的環境中建立運輸囊泡,並對其蛋白質組成進行全面分析。此項研究與香港理工大學姚鍾平教授團隊合作完成。
透過此方法,研究人員識別出依賴AP-1或AP-4運輸的特定運送蛋白,這些蛋白從細胞內的中央分選樞紐——高爾基體的反面網絡運輸。他們確認,蛋白質CAB45為依賴AP-1的貨物,而ATRAP(一種I型血管緊張素II受體相關蛋白)則是AP-4的一種新型貨物。
此研究解開一項長期懸而未決的科學難題,即AP-4運輸複合體如何在毋須依賴網格蛋白(clathrin)的情況下,形成運輸囊泡。團隊發現兩種細胞質因子WDR44與PRRC1在AP-4介導囊泡運輸中發揮關鍵作用。當這些因子被抑制時,AP-4負責運輸的關鍵運送蛋白(如ATG9A與ATRAP)將無法離開細胞器,導致細胞自噬(autophagy)等功能缺陷。
郭玉松強調,本研究不僅揭露AP-1與AP-4的新型貨物及必需輔助因子,更為科學界提供一套強大工具組,可系統性深入解析囊泡運輸機制,為探究相關疾病的病理機制及潛在治療靶點開闢新路徑。
該研究的共同通訊作者為科大郭玉松與理大姚鍾平,第一作者為科大博士後研究員彭子晴。







評論(0)
0 / 255