(香港文匯網記者 郭若溪)近日,中國科學院深圳先進院李紅昌團隊、喻學鋒團隊和李洋團隊等合作的研究成果發表於納米領域國際頂級期刊《自然—納米技術》。研究團隊選取黑磷納米材料為研究對象,通過精細的細胞生物學和分子生物學研究,發現納米材料在細胞內能夠精準靶向特定生物分子,並獲得獨特的生物效應,籍此提出了以分子細胞生物學機製為依託的納米精準分子靶向藥物概念,為納米藥物研發開闢新路徑。

瞄準細胞分裂的「納米導彈」
在本項研究中,研究團隊發現黑磷納米材料可以影響細胞分裂的進行,並以此為機制抑制腫瘤細胞增殖。基於這項發現,團隊提出了腫瘤精準靶向「納米磷療」的新概念,為未來基於黑磷開發新型腫瘤治療藥物奠定了科學基礎。
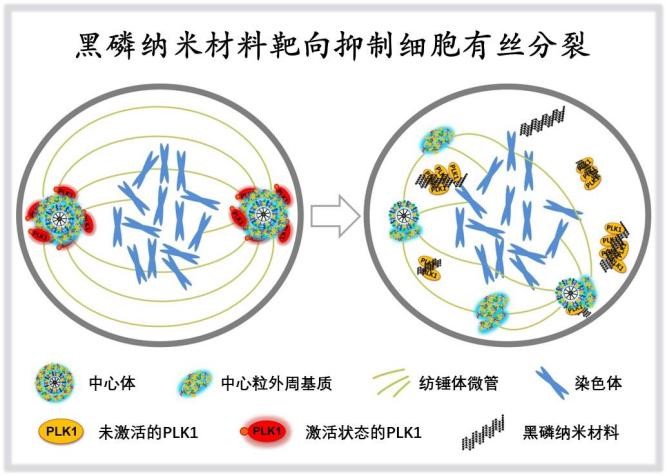
團隊首先使用低濃度黑磷納米材料處理細胞,發現黑磷導致細胞周期停滯在有絲分裂期。隨後,團隊對這一現象背後的機理進行了深入挖掘,發現黑磷破壞了細胞有絲分裂核心機器---紡錘體的組裝。這一機制被最終確定為黑磷導致細胞分裂停滯的直接原因。
「同生物體內其它生命過程一樣,細胞分裂需要眾多生物分子的參與,其中PLK1激酶是非常關鍵的分子開關,其主要功能是控制紡錘體的組裝和運行。」李紅昌表示,黑磷進入細胞後,通過偽裝成PLK1的作用底物,吸引了大量PLK1蛋白與之結合,並使這些PLK1活性喪失,進一步造成紡錘體錯誤組裝,最終阻斷了細胞分裂的正常進行。基於這一機制,黑磷納米材料被賦予了基本的抗腫瘤藥物性質。在隨後的動物實驗中,研究團隊利用小鼠荷瘤模型,進一步證實了黑磷的確具備優異的抗腫瘤效果。
跨學科深度融合
在此次研究過程中,研究團隊充分發揮了學科交叉的特色,自發組成了一支材料學與生物學交叉研究隊伍,成功讓「材料」與「生物」發生深度融合。
「在實際研究過程中,單個課題組很難做到『既懂材料,又通生物』,因此對類似橫跨多個學科的課題,往往難以持續深入地進行,大多研究只能是『淺嘗輒止』。」李紅昌表示,通過「材料人」和「生物人」之間不停地「思想碰撞」和持續地「互通有無」,項目組最終發現了無機單質納米磷材料影響細胞分裂的重要現象,並深入解析了背後的分子細胞機制,這是深圳先進院堅持「學科交叉」理念和秉承「面向世界科技前沿」導向而產生的又一個代表性科研成果。
李紅昌課題組副研究員邵喜明和研究助理丁智昊為論文並列第一作者,李紅昌研究員,喻學鋒研究員和李洋副研究員為論文共同通訊作者,中國科學院深圳先進技術研究院為唯一的第一和通訊作者單位。







評論(0)
0 / 255